NOTÍCIAS
CORONAVÍRUS
#EnergiaNews
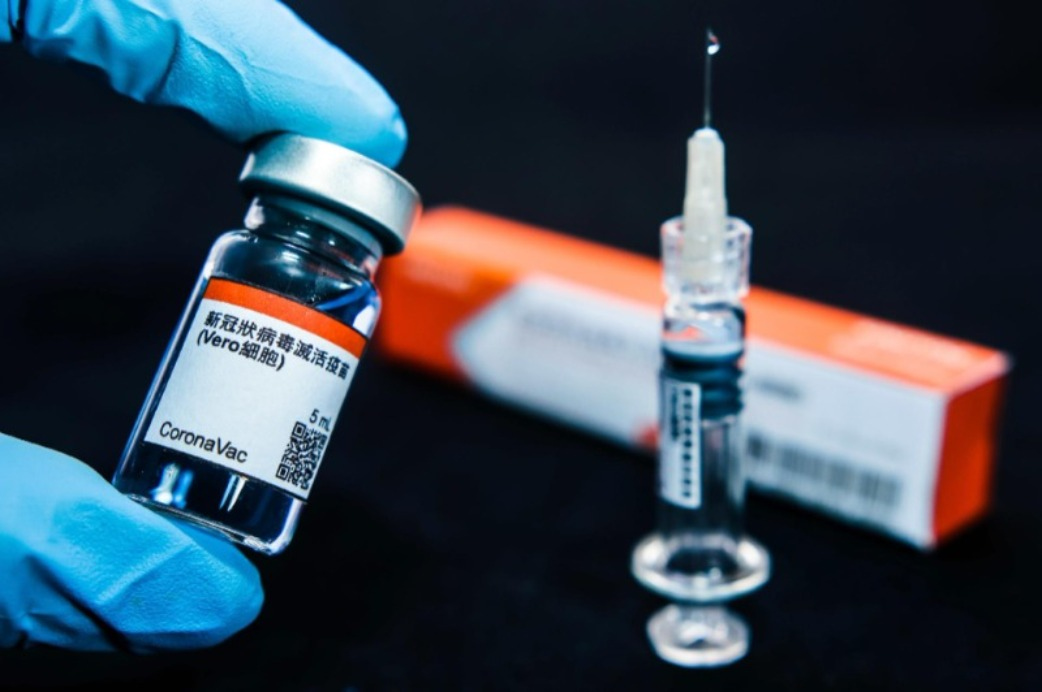
(Crédito: Cadu Rolim/ Fotoarena /Estadão Conteúdo)
O governo da cidade de São Paulo e o Instituto Butantan anunciaram nesta quarta-feira (23) que a vacina CoronaVac, contra o novo coronavírus, produzida em parceria com a SinoVac, apresentou segurança e eficácia em sua fase 3 de testes para pedir registro de uso emergencial. A porcentagem não foi divulgada a pedido do laboratório chinês. A Anvisa (Agência Nacional de Vigilância Sanitária) só deve receber os dados em até 15 dias, onde irá analisar as informações e decidir se aprova ou não o imunizante no Brasil.
O diretor do Instituto Butantan, Dimas Covas, explicou o porquê % da eficácia não foi anunciada. Segundo ele, foi um pedido da SinoVac, previsto em contrato. Isso porque o objetivo é que os dados sejam comparados a resultados de pesquisas em outros países, evitando que o imunizante tenha diferentes índices de eficácia anunciados.
“Essa solicitação da SinoVac tem respaldo no contrato e só podemos divulgar esse número em conjunto. E vamos fazer no tempo oportuno. Esperamos que seja o mais rápido possível”, declarou Dimas, que garantiu que isso não irá interferir no processo de aprovação das vacinas.
O Secretário de Saúde de SP, Jean Gorinchteyn, também anunciou que a porcentagem de eficácia é suficiente para a aprovação.
"Atingimos a superioridade da eficácia da vacina do Instituto Butantan com a SinoVac para covid-19. Atingiu-se aí os índices exigidos tanto pela Anvisa quanto pela OMS nos estudos de fase 3. Isso permitirá com que evitemos a morte de milhares de pessoas, não só no país, mas em todo mundo", anunciou.
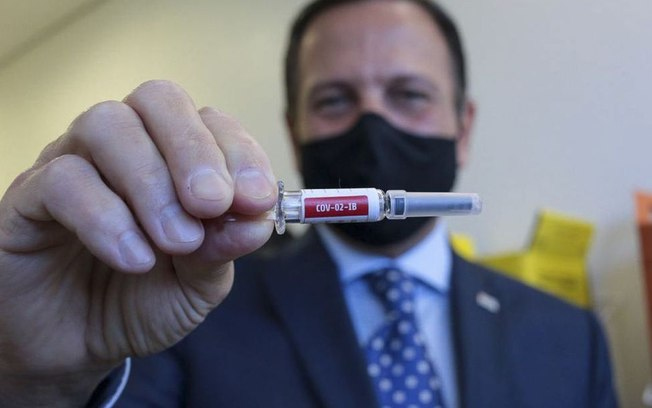
(Foto: Divulgação / Governo de São Paulo)
Jean foi questionado se a falta de divulgação da eficácia aconteceu por conta de uma decepção no resultado. Ele negou e disse que o adiamento demonstra isonomia nos dados:
"Quando os estudos foram começados, nosso objetivo é que a eficácia fosse superior a 50%. Se fosse 51% para nós já era importante, principalmente no momento em que vivemos uma crise sanitária. Uma vacina que jpa represente essa mínima superioridade já e um momento de festejar. O fato disso (adiamento) acontecer transmite isonomia, para que uma empresa possa dizer que todo estudo tem o mesmo percentual de eficácia em qualquer lugar do mundo. É isso que a própria empresa entendeu. Ela quer isonomia, quer que todos os resultados sejam iguais, sem nenhuma disparidade”, explicou.
O Instituto Butantan aproveitou e disse que os testes demonstraram baixa frequência de reações adversas.
"A CoronaVac tem um excelente perfil de segurança com manifestações adversas leves, em uma frequência muito baixa. A reação mais presente é a dor no local da injeção entre o grupo vacinal e o grupo que recebeu o placebo”, anunciou Dimas.
O diretor ainda foi questionado sobre como está o contato com a Anvisa, e ele respondeu:
"Alguns minutos antes de vir para essa coletiva eu falei com Doutor Gustavo Mendes, o diretor da área em que discutimos os estudos. Liguei dando a notícia do que seria feito na coletiva e confirmando que estão, neste momento, a Anvisa e o Butantan, em reunião técnica. Ele me fez um pedido, que avisasse com certa antecedência quando esses dados estivessem sendo disponibilizados para Anvisa, para que ele se preparasse para fazer a análise o mais rapidamente possível. Claro que vamos fazer isso”, garantiu.
FONTE: UOL
ÚLTIMAS
+LEIA TAMBÉM: Anvisa certifica farmacêutica chinesa responsável pela produção da CoronaVac
+LEIA TAMBÉM: Pfizer diz que análise inicial mostra que a vacina da COVID-19 é 90% eficaz