NOTÍCIAS
CORONAVÍRUS
#EnergiaNews
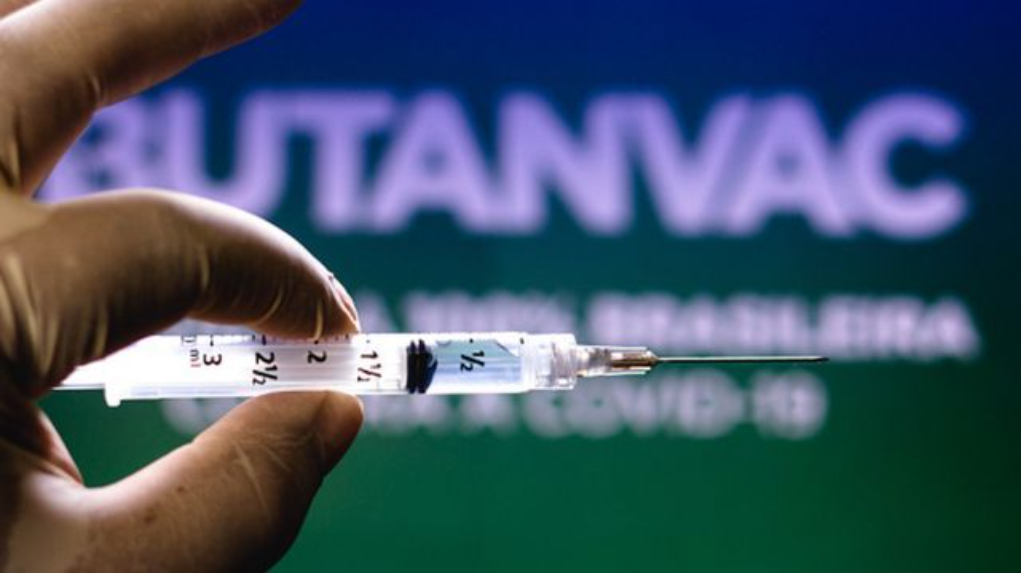
(Foto: Getty Imagens)
Nesta sexta-feira (23), o Instituto Butantan enviou um pedido à Anvisa (Agência Nacional de Vigilância Sanitária) para dar inicio aos testes da Butanvac, vacina contra a Covid-19 produzida no Brasil, em humanos. A notícia foi divulgada pelo vice-governador de São Paulo, Rodrigo Garcia, durante uma coletiva no Palácio dos Bandeirantes.
"Nossa expectativa é de que a Anvisa faça uma análise detalhada mas com a urgência necessária em uma pandemia", disse.
"A vacina será muito rapidamente produzida aqui no Brasil. Teremos uma capacidade enorme de produção, a partir da próxima semana”, afirmou Dimas Covas, diretor do Butantan. "A nossa fábrica que produz a vacina da gripe está liberada para iniciar a produção da Butanvac”, acrescentou.
Covas ainda informou que a previsão é de que até o mês de junho ou julho, cerca de 40 milhões de doses desse imunizante aguardarão o estudo clínico.
"É um estudo de 20 semanas, mas a partir da 16ª poderemos ter resultados de análise primária", afirmou.
A Butanvac é a primeira vacina fabricada no Brasil, sem necessitar de importação de insumos de outros países.
Dimas Covas ainda destacou que o estudo seguirá o padrão determinado pelas demais vacinas.
"Tem marcadores imunológicos, parâmetros de segurança. Vamos analisar se a vacina traz algum tipo de efeito adverso, estudar as pessoas que vão receber e comparar com as demais vacinas existentes. Com isso, temos condições de pedir o uso emergencial. A população-alvo será de adultos", disse o diretor do instituto.

(Foto: Divulgação)
COMO VAI FUNCIONAR OS TESTES?
Assim que a Anvisa autorizar, a vacina passará por três fases de testes.
FASE 1: O objetivo é demonstrar a segurança do imunizante em humanos. Nessa fase é analisada a segurança da tecnologia usada para a produção da vacina.
FASE 2: Definir a reposta imunológica despertada pela vacina.
FASE 3: Essa fase observa a eficácia da vacina demonstrada perante a vida real, quando expostos ao vírus, quantos dos participantes dos testes adoeceram ou não, se tiveram sintomas leves ou moderados e se houve necessidade de internação.
POR: Tamiris Felix
ÚLTIMAS
+LEIA TAMBÉM: Butantan afirma que a vacina ButanVac foi desenvolvida com base em tecnologia de hospital de NY
+LEIA TAMBÉM: Nova vacina chinesa tem autorização da Anvisa para ser testada no Brasil
+LEIA TAMBÉM: Governo de SP anuncia vacinação de idosos de 63 e 64 anos a partir do dia 29 de abril